
Use esse conteúdo a seu favor e esteja apto a criar produtos mais potentes e eficazes no clareamento cutâneo
Existe uma variedade de produtos comercialmente disponíveis para o clareamento cutâneo. Clinicamente, estes produtos também são utilizados para o tratamento de desordens hiperpigmentares, tais como o melasma. Cada produto contém uma combinação de diferentes ativos, cada qual com um mecanismo de ação diferente sobre as etapas da síntese de melanina (melanogênese). Deste ponto em diante, a melanogênese será explanada de forma aprofundada, de maneira a se permitir o entendimento dos mecanismos de ação dos ativos clareadores disponíveis e de possíveis futuros alvos ainda em estudo.
A melanogênese
A coloração da pele humana é percebida em sua parte mais externa: a epiderme, onde os melanócitos, células responsáveis pela produção de melanina, estão localizados. Com a exposição à radiação ultravioleta (UV), a melanogênese é aumentada pela ativação de uma enzima chave: a tirosinase.
A tirosinase é uma glicoproteína localizada na membrana dos melanossomos, que são vesículas presentes no interior dos melanócitos. Estruturalmente, a tirosinase possui um domínio catalítico voltado para o interior do melanossomo, seguido de um pequeno domínio transmembrana e um domínio voltado para o citoplasma. No domínio catalítico, resíduos do aminoácido histidina se ligam aos íons cobre, necessários para a atividade da tirosinase. A melanogênese, portanto, ocorre no interior dos melanossomos, onde dois tipos de melanina são sintetizados: a eumelanina, um polímero insolúvel e de coloração marrom escura a negra, e a feomelanina, um polímero avermelhado ou amarelado e que contém enxofre em sua composição.
O papel da tirosinase é o de catalisar as duas primeiras reações da melanogênese:
- A hidroxilação da L-tirosina, formando L-dihidroxifenilalanina (L-DOPA),
- A oxidação de L-DOPA a L-dopaquinona.
Apesar de a L-tirosina ser o principal bloco para a construção a melanina, ela só pode ser transportada para o interior dos melanossomos por difusão facilitada. No entanto, a L-fenilalanina é ativamente transportada para o interior dos melanossomos: a enzima fenilalanina hidroxilase (PAH) é responsável pela conversão da L-fenilalanina em L-tirosina, garantindo sua concentração no interior dos melanossomos.
Além da radiação UV, outro fator que pode ativar a ação da tirosinase, ainda que indiretamente, é a enzima tirosina hidroxilase isoenzima 1 (TH1). A TH1 também atua na conversão da L-tirosina a L-DOPA (reação 1). A L-DOPA, por sua vez, atua como um cofator para a tirosinase.
Após a formação da L-dopaquinona, as reações que compõem a melanogênese podem seguir por dois caminhos distintos, em que um leva à formação da eumelanina e, o outro, leva à formação da feomelanina. No caminho da eumelanina, a L-dopaquinona é convertida, espontaneamente, à leucodopacroma e, em seguida, à dopacroma. A dopacroma, por sua vez, pode ser convertida em novos produtos por dois caminhos distintos:
- Conversão espontânea a 5,6-dihidroxiindol
- Conversão enzimática a 5,6-dihidroxiindol-2 ácido carboxílico
A enzima responsável pelo segundo caminho é a dopacroma tautomerase (DAT), também conhecida como tyrosin-related protein 2 (TRP-2).
O 5,6-dihidroxiindol, então, é convertido espontaneamente a indol-5,6-quinona e, o 5,6-dihidroxiindol-2 ácido carboxílico, converte-se em sua quinona correspondente por meio da enzima tyrosin-related protein 1 (TRP-1). A polimerização dos indóis e das quinonas gera a eumelanina.
A formação da feomelanina é uma ramificação da formação da eumelanina. Sua síntese é dependente da presença de cisteína, que é ativamente transportada para o interior dos melanossomos. Inicialmente, a L-dopaquinona reage com a cisteína, formando a cisteinil-dopa. Esta é a molécula inicial de uma cascata de reações que levam à formação da feomelanina. A Figura 1 resume todos os passos da melanogênese.

Figura 1: A melanogênese. Adaptado de Gillbro e Olsson, 2011 (1).
A regulação redox no interior dos melanossomos é crucial para o balanço entre a formação de eu e feomelanina, sendo este determinado, diretamente, pela glutationa reduzida (GSH). Altas concentrações de GSH levam à formação de eumelanina, enquanto que baixas concentrações de GSH desviam a melanogênese para a formação de feomelanina. A melanina, per se, também possui uma ação na homeostase oxidativa da pele: a eumelanina é capaz de sequestrar e quelar radicais livres derivados de oxigênio e de carbono, ao passo que a feomelanina não possui estas habilidades e, ainda, é capaz de gerar radicais livres na presença de UV. A melanina, por sua carga negativa, é capaz de se ligar a aminas e a metais pesados.
Outras regulações da melanogênese
Há alguns anos, a descoberta do gene que codifica para o fator de transcrição MITF (microphtalmia-associated transcription fator) promoveu o estudo da regulação gênica em melanócitos. É provável que o MTIF seja o coração de uma rede regulatória que controla a sobrevivência, a proliferação e a diferenciação celular dos melanócitos. Além disso, este fator de transcrição regula a pigmentação por seus efeitos sobre a transcrição da tirosinase, da TRP-1 e da TRP-2. Também se demonstrou que o MTIF tem um papel sobre a proteína Rab27A, importante no transporte dos melanossomas.
À parte do MTIF, existem vários fatores parácrinos que podem estimular a melanogênese, tais como os peptídeos derivados da pró-opiomelanocortina (POMC) como α-MSH, β-MSH e ACTH. A POMC é produzida pelos queratinócitos quando expostos à radiação UV. Os peptídeos derivados da POMC exercem seus efeitos por um mecanismo dependente de AMP cíclico (AMPc) quando se ligam ao receptor MC1R. Este receptor é acoplado a proteínas Gs, que atuam como mensageiras estimulatórias da melanogênese.
As proteínas Gs levam à ativação da adenilil ciclase (AC), que por sua vez, produz AMPc a partir do ATP. O AMPc ativa uma proteína quinase (PKA), que fosforila enzimas, canais iônicos e uma série de outros fatores regulatórios, eventualmente alterando a expressão gênica. Um destes fatores, denominado CREB, ativa a transcrição de MITF que, por sua vez, ativa a transcrição das enzimas envolvidas na melanogênese em cultura de melanócitos. Uma representação gráfica desta regulação pode ser vista na Figura 2. À parte desta regulação, descobriu-se que, em especial, a α-MSH não só aumenta a síntese de melanina por meio dos receptores MC1R, como também por se ligar à proteína 6BH4, inibidora competitiva da tirosinase.
Além dos peptídeos derivados da POMC, outros fatores parácrinos como a endotelina-1, as prostaglandinas e as catecolaminas também podem exercer efeitos importantes sobre a coloração da pele.
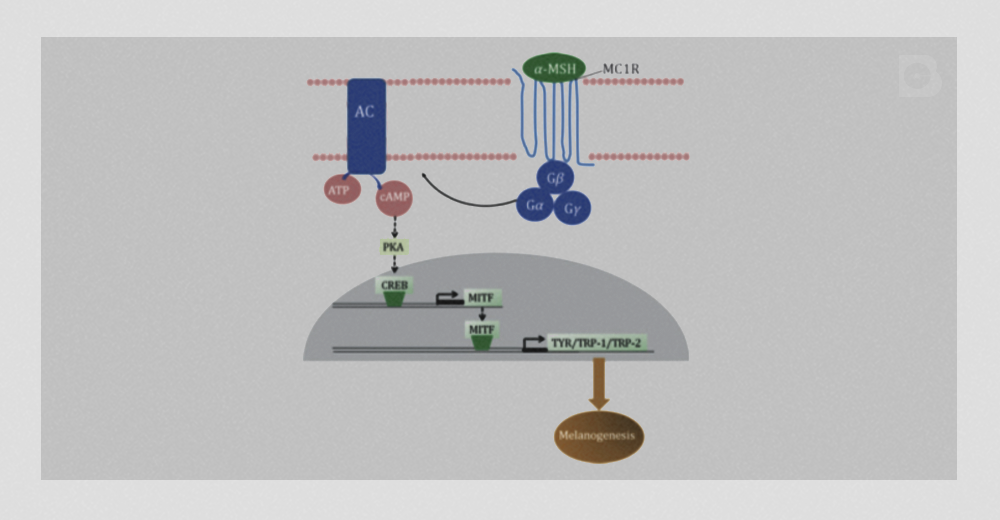
Figura 2: Regulação da melanogênese via MC1R, AC e MITF. De Gillbro e Olsson, 2011. (1)
Ativos clareadores
Existem várias substâncias que podem reduzir o nível de pigmentação da pele. Os principais mecanismos de atuação destas substâncias residem na inibição da síntese de melanina, principalmente por meio da inibição da tirosinase, na inibição da transferência da melanina aos queratinócitos, na descamação da pele para a remoção do excesso do conteúdo de melanina e na ação antioxidante. A seguir, apresentam-se os ativos de cada uma destas classes.
Inibidores da tirosinase
A tirosinase é o alvo mais comum para o clareamento cutâneo. Os inibidores da tirosinase mais comuns são os compostos derivados de quinonas, tais como a hidroquinona.
A hidroquinona foi o padrão convencional no tratamento de hiperpigmentações por mais de 40 anos. Este ativo pode ser encontrado no trigo, na cerveja no café e em berries. A hidroquinona age por se ligar às histidinas do domínio ativo da tirosinase, além de induzir à geração de espécies reativas de oxigênio, as quais danificam lipídeos e proteínas como a própria tirosinase. Outras ações da hidroquinona estão na depleção da glutationa e na redução da síntese de DNA e RNA com concomitante degradação dos melanossomas e danificação dos melanócitos. Por apresentar alta agressividade, gerando perda de melanócitos e descoloração permanente da pele, a hidroquinona deixou de ser o padrão e foi banido na Europa. Atualmente, empregam-se substitutos em formulações.
Um dos substitutos à hidroquinona é o arbutin, um derivado glicosilado da hidroquinona encontrado em cranberries, blueberries, no trigo e em ervilhas. O arbutin é menos citotóxico que a hidroquinona e inibe a tirosinase por ligação competitiva e reversível, sem influenciar na transcrição de seu mRNA. A ação mais suave do arbutin em relação à hidroquinona é atribuída à sua ligação glicosídica, que deve ser rompida para que ocorra o efeito sobre a tirosinase.
Derivado sintético do arbutin, o deoxiarbutin demonstra-se eficaz e menos citotóxico que os ativos anteriores. A capacidade de inibição da tirosinase é similar à da hidroquinona e à do arbutin, mas o deoxiarbutin age, também, na redução da transcrição do gene que codifica para a tirosinase.
Existem ativos não relacionados a quinonas e que atuam inibindo a tirosinase. É o caso do ácido kójico, isolado de fungos o gênero Acetobacter, Aspergillus e Penicillium. Acredita-se que sua ação se dê por meio da quelação dos íons cobre no sítio ativo da tirosinase, além de inibir a conversão da dopacroma em 5,6-dihidroxiindol-2 ácido carboxílico. Apesar de popular no tratamento do melasma, o ácido kójico pode causar sensibilização, eritema e dermatite de contato.
Outro ativo produzido por microrganismo é o ácido azeláico. Naturalmente encontrado no trigo, no centeio e na cevada, este ativo pode ser produzido pela levedura Pityrosporum ovale e é normalmente empregado no tratamento da acne, da rosácea, da pigmentação cutânea, das sardas, dos nevos e das manchas senis. Seu mecanismo de ação se dá pela ligação a grupamentos amino e ácidos carboxílicos: portanto, deve prevenir a interação da tirosina com a tirosinase, funcionando como um inibidor competitivo.
Por fim, apesar de controversos, vale mencionar os ativos flavonoid-like. Existem cerca de 4000 flavonoides identificados até o momento, apresentando uma variedade de atividades como a anti-inflamatória, a sequestradora de radicais livres e a anti-carcinogênica. Alguns destes flavonoides, como a aloesina, os derivados de hidroxistilbenos e o extrato de licorice são utilizados em formulações para clareamento cutâneo. A aloesina, por exemplo, é capaz de inibir competitivamente a tirosinase e a ação das enzimas TH e DOPA oxidase. Já os hidroxistilbenos, do qual o representante mais conhecido é o resveratrol, podem reduzir a atividade da tirosinase e, ainda, a expressão de MITF. O extrato de licorice, em especial a glabridina presente na fração hidrofóbica, também possui a capacidade de inibir a tirosinase. A controvérsia do uso de compostos flavonoid-like como ativos clareadores reside no fato de que alguns flavonoides promovem o efeito inverso, ou seja, promovem a melanogênese. Alguns exemplos de flavonoides praradoxos são a naringenina, a quercetina, a luteolina e a taxifolina.
Inibição da transferência da melanina
Uma etapa crítica da pigmentação cutânea é a transferência dos melanossomos aos queratinócitos. Embora muito se saiba sobre os melanócitos e os queratinócitos isoladamente, as interações entre estas células ainda carecem de estudo para um maior entendimento. Sugere-se que o receptor protease-ativado 2 (PAR-2) possua um papel importante nessa transferência, de forma que a ativação de PAR-2 implica em aumento da hiperpigmentação. Na epiderme, PAR-2 está presente apenas em queratinócitos, levando-se a crer que a sua ativação aumente a capacidade fagocítica dos queratinócitos e, desta forma, amplie a capacidade de captação de melanossomas por estas células. Acredita-se que os extratos de soja e o leite de soja tenham a capacidade de inibir PAR-2, atuando como agentes clareadores por este mecanismo.
Outro ativo para o qual acredita-se que o mecanismo de ação seja a inibição da transferência de melanossomos aos queratinócitos é a niacinamida. Este composto é a forma biologicamente ativa da vitamina B3 e é um importante precursor dos cofatores enzimáticos NADH e NADPH. Lecitinas e seus conjugados também possuem efeito semelhante, embora a foram de atuação sobre a transferência de melanossomos seja ainda desconhecida.
Descamação da pele e aceleração do turnover celular
Os agentes químicos que promovem a descamação da epiderme também são empregados com a finalidade de redução de manchas devido ao fato de removerem os queratinócitos ricos em melanina. Alguns exemplos de ativos desta categoria são os α-hidroxiácidos e os ácidos salicílico, linoleico e retinóico. Alguns destes ácidos, como o glicólico (o menor dos α-hidroxiácidos) e o linoleico, exibem não só a capacidade esfoliante, como também são capazes de inibir a tirosinase. Acredita-se que os ácidos retinoides ajam sobre a transcrição da tirosinase, reduzindo-a assim como o ácido octadecenodioico, que se liga aos receptores PPAR-γ inibindo os níveis de mRNA e, consequentemente, de tirosinase disponíveis. Em contraste com os ácidos graxos insaturados, os ácidos graxos saturados como o palmítico e o esteárico exibem o efeito oposto, aumentando a atividade tirosinase e a síntese de melanina.
Antioxidantes
A ideia de se utilizarem os antioxidantes para o clareamento da pele vem da hipótese de que o estresse oxidativo gerado pela radiação UV contribui com a ativação da melanogênese. Sabe-se que a tirosinase tem preferência ao íon superóxido (O2- ) em detrimento do oxigênio (O2) e que a radiação UV é capaz de induzir à formação de espécies reativas de oxigênio (EROs) na pele. Os agentes antioxidantes podem, também, interagir com o íon cobre presente no domínio ativo da enzima tirosinase ou com as orto-quinonas formadas durante a melanogênese, impedindo a sua polimerização para a formação de melanina. Ainda, os antioxidantes podem reduzir a foto-oxidação da melanina pré-existente. Alguns dos antioxidantes veiculados em formulações para clareamento cutâneo são as vitaminas E, C e B.
Uma visão geral dos estudos realizados para todos estes ativos clareadores pode ser encontrada na Tabela 1.
| Ativo |
In vitro |
In vivo |
| Hidroquinona |
Inibição da tirosinase, inibição do metabolismo celular envolvendo a síntese de DNA e de RNA. |
Estudos clínicos em pacientes com melasma mostraram a redução da pigmentação. |
| Arbutin Deoxiarbutin |
Inibição da atividade tirosinase e da produção de melanina. Inibição das atividades tirosina hidroxilase e DOPA oxidase. |
Estudos clínicos mostraram um clareamento geral da pele e uma melhora dos lentigos solares após um tratamento de 12 semanas. |
| Ácido kójico e tripeptídeos de ácido kójico |
Inibição da atividade tirosinase. |
Um estudo comparativo entre o ácido kójico e a hidroquinona mostraram resultados semelhantes. |
| Aloesina |
Inibição das atividades tirosinase, tirosina hidroxilase e DOPA oxidase. Sinergia com arbutin. |
Estudo clínico mostrou uma supressão de 34% da pigmentação no antebraço. |
| Resveratrol |
Redução nas atividades promotoras de MITF e tirosinase |
Sem estudos em humanos. Notou-se clareamento da pele de suínos Yucatan, com confirmação histológica. |
| Glabridina (Licorice) |
Glabreno e isoliquiritigenina do extrato de licorice inibem as atividades mono e di-fenolase da tirosinase. |
Ensaios clínicos mostraram resultados excelentes em 90% dos pacientes tratados com creme de liquiritina |
| Soja |
A soja inibe a clivagem do receptor PPAR-2, afeta a organização do citoesqueleto e da superfície celular e reduz a fagocitose em queratinócitos. |
Estudo sobre a pele do rosto fotodanificada mostrou que a soja é superior a aplicação apenas do veículo na melhoria da pigmentação. |
| Niacinamida |
Sem atividade sobre a tirosinase de cogumelos ou sobre a melanogênese em cultura de melanócitos. Inibição entre 35-68% da transferência dos melanossomos em modelo de co-cultura. |
Estudo clínico mostrou melhoria significativa sobre o controle em relação a rugas e linhas finas, sobre pontos de hiperpigmentação e sobre pontos de vermelhidão. |
| α-hidroxiácidos |
Os ácidos glicólico e lático inibiram a formação d e melanina em células de melanoma humano. A tirosinase foi inibida. Não se notam efeitos sobre o mRNA de tirosinase, TRP-1 e TRP-2. |
Estudo com a aplicação de ácido glicólico a 10% em melasma mostrou melhoria em 91% dos pacientes. |
| Ácido retinoico |
Inibição da tirosinase e da expressão de TRP-1 concomitante com a síntese de melanina |
Estudo sobre o clareamento total da pele facial mostrou um clareamento em 68% dos pacientes. |
| Vitamina C |
Supressão da formação de melanina em tirosinase purificada e em melanócitos. |
A aplicação de creme com magnesium-L-ascorbyl-2-phosphate resultou em clareamento da pele em 19 de 34 pacientes com cloasma ou manchas senis. |
| Ácido octadecenodioico |
Redução em mRNA de tirosinase e expressão proteica concomitante com a inibição da melanogênese. |
Uniformização do tom da pele e clareamento cutâneo em geral. |
Tabela 1: Resultados dos estudos realizados in vitro e in vivo para os ingredientes clareadores. De Gillbro e Olsson, 2011.
Conjugações para aumentar a viabilidade e o efeito dos ativos clareadores
Muitos ativos clareadores possuem problemas de citotoxicidade ou de instabilidade durante o armazenamento. Em decorrência disso, algumas moléculas vêm sendo conjugadas para se atingir o efeito desejado. O ácido kójico, por exemplo, vem sendo conjugado por meio da conversão da hidroxila C7 em um éster, em um glicosídeo, um derivado de aminoácido ou em derivados de tripeptídeos. Além da estabilidade, a própria atividade pode ser melhorada: a conjugação do ácido kojico com aminoácidos aumenta a eficácia da inibição da tirosinase em até 90%. Outra molécula que vem sendo conjugada a ativos clareadores como o ácido kójico e a vitamina C é o 3-aminopropil-dihidrogenofosfato (3-APPA) que, além de melhorar a estabilidade dos ativos claradores, promove a permeação destas moléculas na pele, o que resulta em maior eficácia de clareamento.
Hipóteses para novos alvos de ativos clareadores
Estudos vêm sendo realizados para a detecção de novos alvos para o clareamento cutâneo. Um deles é o receptor β2-adrenérgico (β2-AR), presente em queratiócitos humanos. Em ratos, foi proposto que este receptor possa ser um ponto alternativo à via das POMCs para a ativação da melanogênese. Desta maneira, antagonistas dos receptores β2-AR seriam bons candidatos a ativos clareadores cutâneos.
Novas formas de inibição da MITF também vem sendo propostas. Estudos mostraram que receptores glutaminérgicos afetam a expressão de MITF, de forma que, quando bloqueados, uma redução drástica de MITF acontece, além de uma modificação da morfologia dos melanócitos que culmina com a retração dos dendritos. Em ratos, a superexpressão do receptor glutaminérgico 1 ocasionou a hiperproliferação de queratinócitos, de forma que inibidores deste tipo de receptor também são potenciais candidatos a ativos clareadores.
O 6BH4 é um cofator para as enzimas PAH e TH, além de ser um inibidor alostérico da tirosinase: desta maneira, o 6BH4 possui um papel fundamental no controle da melanogênese. Análogos do 6BH4 vêm sendo investigados como novos inibidores da tirosinase.
Por último, alguns estudos vêm demonstrando que os melanócitos podem ser responsivos a estrógenos, embora não se tenha comprovado, cientificamente, o papel do estrógeno na hiperpigmentação cutânea. Por outro lado, a dehidroepiandrosterona reduziu a pigmentação cutânea em cerca de 10% nas mulheres que administraram esta substância por via oral.
Embora não se tenham dados conclusivos, percebe-se que a regulação hormonal exerce efeitos sobre a pigmentação cutânea, porém o papel dela deve ser investigado com mais profundidade para a proposição de ingredientes que atuem sobre os hormônios.
Você gostou desse artigo?
Espero que sim e adoraria saber sua opinião!
Compartilhe sua opinião nos comentários e não deixe de se inscrever em nossa lista de emails para receber novos artigos.
O objetivo desse artigo é contribuir para a elevação do nível técnico de profissionais da área. Para qualquer orientação procure sempre um profissional habilitado como um dermatologista ou farmacêutico.
Quer ter independência para criar formulações cosméticas do zero e nunca mais reproduzir fórmulas prontas?
A Escola Vinia possui programas presenciais e online com o método mais completo para aprender a criar formulações dos produtos cosméticos mais procurados pelos consumidores, com abordagens diretas e focadas nos pontos essenciais para se fazer um ótimo trabalho como formulador e se destacar na criação de fórmulas cosméticas.
São cursos comigo que te ensinam:
- Principais ingredientes cosméticos na criação de produtos.
- Como formular cremes, loções, manteigas corporais e séruns.
- Como formular shampoos e sabonetes líquidos.
- Como formular condicionadores, cremes para pentear e máscaras hidratantes.
- Como formular fotoprotetores estabilizados e eficazes.
- Como formular cosméticos para pele delicada (pele sensível, idosos, gestantes e crianças).
Referências:
[1] J. M. Gillbro and M. J. Olsson. The melanogenesis and mechanisms of skin-lightening agents – existing and new approaches. International Journal of Cosmetic Science, 2011, 33, 210–221.

Como suspender partículas em formulações cosméticas

Óleo essencial e óleo vegetal: principais diferenças e aplicações no P&D de cosméticos

Saponificação: domine essa reação e fature com esse processo criando barras de limpeza…

O impacto das embalagens na estabilidade de produtos cosméticos
Olá,
o que você achou deste conteúdo? Conte nos comentários.













[…] enzima tirosinase ~criei um post explicando de forma mais completa como ocorre a pigmentação. Clique aqui e leia~. Logo, uma via possível de inibição da hiperpigmentação é a inibição dessa enzima. Foi […]